BDのグループ会社である株式会社メディコン(本社:大阪府大阪市、代表取締役社長 阿知波 達雄)は、2022年7月28日に、末梢動脈疾患(PAD)における大腿膝窩動脈の再狭窄を抑制する「Lutonix™ RXドラッグコーティングバルーンカテーテル(大腿膝窩動脈用)」(以下Lutonix™ RX)において、新たにステント内再狭窄病変と30cmまでの長病変の適応について薬事承認を取得し、2022年9月1日に保険償還を取得しました。
下肢末梢動脈疾患は、加齢に伴う動脈硬化などが原因で、足の血管が細くなることや完全に詰まることで、血流が悪くなる疾患で、症状が進行すると足のしびれや痛みが強くなり、歩行が困難になることもあります。さらに重症化すると足を切断しなくてはならないケースや、歩けないことで動脈硬化が進行し、心筋梗塞、脳卒中にも繋がるなど命に関わることもある疾患です。
こうした虚血性の下肢末梢動脈疾患における大腿膝窩動脈病変の治療には、治療後の再狭窄を抑制するために、バルーン表面に薬剤をコーティングしたドラッグコーティングバルーンカテーテル(DCB)が、有効性、安全性の高い治療デバイスとして、多くの医療機関で採用されています。2020年2月より全国販売を開始したLutonix™ RXは、狭窄や閉塞した動脈内の病変をバルーンで拡張し、再狭窄抑制効果を有する薬剤であるパクリタキセルを病変部に移行させることで再狭窄を抑制します。一方で、従来のLutonix™ RXの適応病変長は15cmまでであり、より長い病変への適応はありませんでした。
今回新たに取得した適応拡大の薬事承認により、30cmまでの長病変に適応するとともに、ステント内再狭窄病変についてもLutonix™ RXが使用できるようになりました。これにより、より幅広い患者さんの治療に対応することが可能となります。またLutonix™ RXは、日本における一般的な術式に適合するように、0.014 inchガイドワイヤ対応のRapid Exchangeタイプのバルーンカテーテルをベースバルーンとして採用しています。このことで、本製品が日本の術者と患者さんにとって、安全で低侵襲な治療となることに貢献できればと考えています。
Lutonix™ RXドラッグコーティングバルーンカテーテルについて
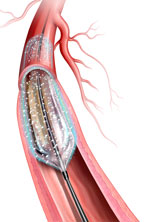 Lutonix™ RX(イメージ図)
Lutonix™ RX(イメージ図)
「Lutonix™ RX ドラッグコーティングバルーンカテーテル (大腿膝窩動脈用)」は、2020年2月に株式会社メディコンが発売した末梢動脈疾患(PAD)による、大腿膝窩動脈の再狭窄を抑制するドラッグコーティングバルーンカテーテルです。狭窄や閉塞した動脈の病変部にバルーンを配置して、バルーン表面に塗布した薬剤「パクリタキセル」が血管壁に移行する仕組みです。日本での治療において標準的に使用されている0.014 inch径のガイドワイヤに適合し、術者にとって取り回しの良いRapid Exchange型のバルーンカテーテルを採用しています。
*1 製品添付文書(2022年7月28日改訂、第7版)より抜粋
製造販売元:株式会社メディコン